Patrick Omoumi, stellvertretender Herausgeber von European Radiology und Radiologe am Universitätsspital Lausanne, hat beim ESR Annual Leadership Meeting 2025 in Cannes eine Frage in den Mittelpunkt gestellt, die viele Abteilungen derzeit umtreibt: Wie gelingt der Schritt von der Begeisterung für Künstliche Intelligenz zur strukturierten, sicheren und wirtschaftlich tragfähigen Implementierung im klinischen Alltag?
Zwischen Versprechen und Evidenz
KI verspricht beschleunigte Workflows, bessere Bildqualität und effizientere Befundung. Besonders generative Modelle zur MRT-Beschleunigung gelten als Hoffnungsträger: kürzere Akquisitionszeiten bei gleichbleibender oder sogar verbesserter Bildqualität. Doch Omoumi mahnt zur wissenschaftlichen Nüchternheit. Prospektive Studien zur klinischen Leistungsfähigkeit sind bislang begrenzt; ökonomische Analysen zu KI einkaufen – aber richtig. Wie Radiologien die Lücke zwischen Vision und Versorgungsrealität schließen, ist hingegen selten. Zudem sind halluzinatorische Artefakte, also algorithmisch erzeugte, klinisch jedoch nicht reale Strukturen, ein ernstzunehmendes Risiko mit potenziell falsch-positiven oder falsch-negativen Befunden.
Die Kernbotschaft: Technische Machbarkeit ersetzt keine klinische Evidenz.
Beschaffung ist ein Prozess – kein Klick im App-Store
Omoumi strukturiert den KI-Einkauf in drei Phasen: Pre-Trial, Trial und Production. Jede Phase erfordert die enge Zusammenarbeit zwischen Medizin, IT, Ingenieurwesen, Rechtsabteilung und Klinikmanagement.
◾ Pre-Trial: Am Anfang steht eine saubere Bedarfsanalyse. Welches klinische Problem soll gelöst werden? Wer sind die Endanwender? Geht es um Forschung oder um Routineversorgung? Ebenso wichtig ist das Verständnis der IT-Prozesse: Handelt es sich um Standard-Medizinsoftware oder gibt es spezifische KI-Regularien? Auch strategische Fragen gehören hierher: Build or buy? Einzelprodukt oder Plattformlösung im Sinne eines App-Stores? Produktregister wie ACR AI Central können bei der Identifikation helfen. Vertragsgestaltung, Anforderungskatalog und Ausschreibung sollten sich an etablierten Leitlinien wie ECLAIR und Multi-Society-Statements orientieren.
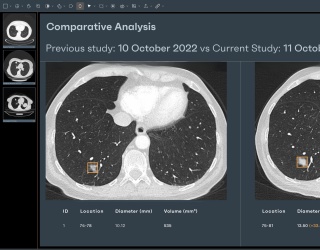
◾ Trial: In der Testphase geht es um reale Performance. Wie gut integriert sich die Lösung in PACS und RIS? Arbeitet sie im Batch-Modus oder interaktiv? Wie hoch ist die Antwortzeit? Entscheidend ist die Analyse des Performance-Gaps, also der Differenz zwischen den Herstellerangaben und der realen klinischen Leistung. Ebenso relevant sind der Einfluss auf die Befundungszeit, die Zusatzuntersuchungen sowie den Gesamtworkflow.
◾ Production: Der Go-Live markiert nicht das Ende, sondern den Beginn eines kontinuierlichen Monitorings. Wartung, Performance-Drift , Ausfallmodi und die Frage, ob IT oder Radiologie die Verantwortung trägt, müssen vorab klar definiert werden.
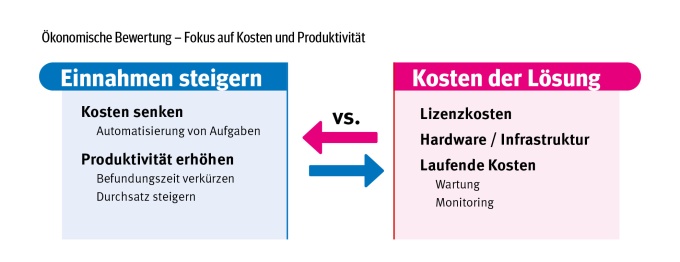
Ökonomie: Mehr als Lizenzkosten
Omoumi unterstreicht, dass die KI-Beschaffung immer auch eine gesundheitsökonomische Bewertung erfordert. Lizenzmodelle, Hardware, Infrastruktur, Wartung und Monitoring verursachen wiederkehrende Kosten. Demgegenüber stehen potenzielle Ertragssteigerungen, Produktivitätsgewinne und reduzierte Befundungszeiten.
Ein Beispiel ist die automatisierte Landmarkendetektion in der EOS-Bildgebung: Wenn ein Technologe bislang 15 Minuten pro Patient benötigt, davon die Hälfte für Post-Processing, kann Automatisierung theoretisch die Fallzahl verdoppeln. In einem Szenario mit 5.000 Fällen pro Jahr ließe sich so perspektivisch sogar die Finanzierung eines neuen Systems ermöglichen. Doch Tarifänderungen (z. B. neue ambulante Vergütungssysteme) sowie die Akzeptanz beim Personal beeinflussen die tatsächliche Wirtschaftlichkeit.
Produktivität messbar machen
Ein weiteres Fallbeispiel: KI-unterstützte Wirbelsäulenbefundung. In einer Studie mit acht Radiologen sank die Interpretationszeit pro Fall von 124 bis 274 Sekunden auf 47 bis 71 Sekunden – also rund drei Minuten Zeitgewinn pro Untersuchung. Gleichzeitig verbesserte sich die Interobserver-Übereinstimmung sig-nifi kant (von κ = 0,39 auf bis zu 0,71). Solche Daten sind mehr als nur akademische Kennzahlen.
Sie bilden die Grundlage für Kosten-Effektivitäts-Analysen, etwa im Sinne von Cost-Effectiveness- oder Cost-Utility-Ansätzen (QALYs). Gleichzeitig stellt sich die Frage: Wer trägt die Kosten? In Fee-for-Service-Systemen lassen sich Softwarelösungen schwer in Einzelleistungen abteilen; häufig verbleibt die wirtschaftliche Last beim Radiologen. Value-based-Modelle könnten hier neue Anreizstrukturen schaffen.
Notaufnahme als Realitätstest
Besonders komplex erwies sich die Evaluation einer kommerziellen Frakturerkennungssoftware in der Notaufnahme. Wie geht man mit „zweifelhaften“ KI-Ergebnissen um? Verlängert sich dadurch die Analysezeit? Müssen zusätzliche Aufnahmen erfolgen? Auch die Bewertung von Fehlklassifikationen ist differenziert zu betrachten: Ein übersehener Schenkelhalsbruch ist nicht gleichbedeutend mit einer verpassten Rippenfraktur. Demografische Faktoren und die Frakturlokalisation beeinflussen den klinischen Impact erheblich. Hinzu kommen interdisziplinäre Effekte: Wenn der ER-Workflow schneller wird – wer profitiert ökonomisch davon?
Von der Effizienz zur Wertschöpfung
Omoumi verweist auf etablierte Wirksamkeitsmodelle wie das von Fryback und Thornbury: von technischer Genauigkeit über diagnostische und therapeutische Effekte bis hin zu patientenbezogenen Outcomes und gesellschaftlicher Kosteneffektivität. KI muss sich auf allen Ebenen messen lassen – nicht nur an Sensitivität und Spezifität. Value-Assessment-Frameworks gehen noch weiter: Sie integrieren Evidenzqualität, Ethik, Equity und gesellschaftliche Perspektiven. Damit wird klar: Der „Wert“ einer KI-Lösung ist kontextabhängig – aus Sicht von Patienten, Klinik, Kostenträgern und Gesellschaft .
Fazit: Struktur schlägt Euphorie
It’s complicated in practice – so bringt Omoumi die Realität auf den Punkt. Erfolgreiche KI-Beschaffung erfordert:
◾ klare Bedarfsdefinition
◾ Einbindung aller Stakeholder
◾ realistische Leistungsbewertung
◾ transparente Kostenanalyse inklusive versteckter Aufwände
◾ definiierte KPIs für Performance und Wert
Für Radiologien bedeutet das: KI ist kein Gadget, sondern ein strategisches Investitionsprojekt. Wer strukturiert vorgeht, Evidenz ernst nimmt und ökonomische sowie organisatorische Effekte mitdenkt, kann die Lücke zwischen Theorie und klinischer Praxis tatsächlich schließen.