Zulassungsantrag für Gadoquatrane in Japan eingereicht
- Antrag auf Marktzulassung von niedrig dosiertem Kontrastmittel Gadoquatrane für kontrastmittelverstärkte MRT-Untersuchungen aller Körperregionen bei Erwachsenen und Kindern, einschließlich Neugeborenen
- Die beantragte Dosis entspricht einer 60-prozentigen Gadoliniumreduktion im Vergleich zu standardmäßigen makrozyklischen Kontrastmitteln auf Gadoliniumbasis mit einer Dosierung von 0,1 mmol Gadolinium pro Kilogramm Körpergewicht
- Japan verfügt pro Kopf über die weltweit höchste Anzahl an MRT-Scannern, mit jährlich etwa 20 Millionen Untersuchungen
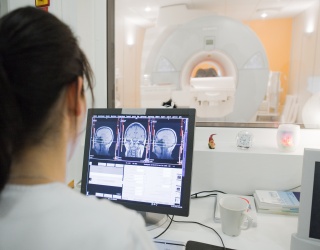
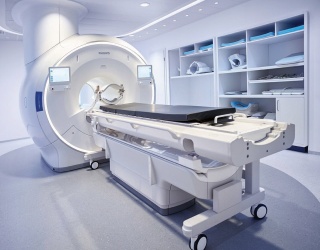
Bayer gab die Einreichung eines Zulassungsantrags beim japanischen Ministerium für Gesundheit, Arbeit und Soziales (MHLW) für das in der Entwicklung befindliche Kontrastmittel Gadoquatrane zur Kontrastverstärkung in der Magnetresonanztomographie (MRT) bekannt. Gadoquatrane soll bei der Erkennung und Visualisierung bekannter oder vermuteter Erkrankungen in allen Körperregionen und des zentralen Nervensystems (ZNS) bei Erwachsenen und Kindern, einschließlich Neugeborenen, eingesetzt werden. Die beantragte Dosis von 0,04 mmol Gadolinium (Gd) pro Kilogramm Körpergewicht entspricht einer Gd-Reduktion um 60 Prozent im Vergleich zur Standarddosis makrozyklischer Kontrastmittel von 0,1 mmol Gd/kg Körpergewicht.
„Als führendes Unternehmen in der Radiologie bringen wir Innovationen zum Wohle der Patienten voran – dazu zählen auch mögliche Optionen zur Reduktion der Gadoliniumdosis“, sagte Dr. Konstanze Diefenbach, Leiterin der Forschung und Entwicklung in der Radiologie bei Bayer. „Die Zulassung von Gadoquatrane würde Radiologen in Japan eine niedrigdosierte Option zur Unterstützung der Diagnose ihrer Patienten bieten. Eine Niedrigdosisoption könnte insbesondere für Patienten, die im Laufe ihres Lebens mehrere MRT-Untersuchungen erhalten, sowie für Kinder von Nutzen sein.“
Derzeit sind in Japan keine niedrigdosierten MRT-Kontrastmittel verfügbar. In Zeiten einer alternden Bevölkerung und einer Zunahme chronischer Erkrankungen wie Krebs und Herzkrankheiten verfügt Japan über die weltweit höchste Anzahl an MRT-Geräten pro Kopf. Jährlich finden dort etwa 20 Millionen MRT-Untersuchungen statt.
Die Einreichung des Zulassungsantrags für Gadoquatrane beim MHLW basiert auf positiven Daten der zulassungsrelevanten Phase-III-Studien QUANTI, in denen die Wirksamkeit und Sicherheit von Gadoquatrane in einem breiten Indikationsspektrum bei erwachsenen und pädiatrischen Patienten untersucht wurde. Erste Ergebnisse der Phase-III-Studie QUANTI CNS wurden auf dem European Congress of Radiology (ECR) im Februar dieses Jahres vorgestellt. Weitere Ergebnisse sollen auf kommenden wissenschaftlichen Kongressen präsentiert werden. Die Einreichung in Japan ist der erste Antrag auf Marktzulassung für Gadoquatrane. Weitere Zulassungsanträge bei Gesundheitsbehörden weltweit sind für die kommenden Monate geplant.
Über das Phase-III-Entwicklungsprogramm QUANTI
Das zulassungsrelevante klinische Entwicklungsprogramm QUANTI untersuchte Gadoquatrane in einer Dosierung von 0,04 mmol Gd/kg Körpergewicht. Dies entspricht einer um 60 Prozent niedrigeren Gadoliniumdosis im Vergleich zu makrozyklischen Kontrastmitteln mit einer Dosierung von 0,1 mmol Gd/kg Körpergewicht. QUANTI bestand aus zwei großen multinationalen, randomisierten, prospektiven, doppelblinden Crossover- Phase-III-Studien – QUANTI CNS (Zentrales Nervensystem) und QUANTI OBR (Andere Körperregionen) – sowie der pädiatrischen Studie QUANTI Pediatric. Insgesamt nahmen 808 Patienten in 15 Ländern an dem Studienprogramm teil. In Japan waren 27 Prüfzentren beteiligt.
Im Januar 2025 gab Bayer positive Topline-Daten für die QUANTI-Studien bekannt. Die Ergebnisse zeigten, dass Gadoquatrane die primären und sekundären Wirksamkeitsendpunkte der Studien zur Bewertung der Visualisierungsparameter und Läsionserkennung erreichte und damit eine nicht unterlegene Wirksamkeit gegenüber den Vergleichspräparaten der Studie bewies. Das beobachtete Sicherheitsprofil von Gadoquatrane war mit den Daten für die makrozyklischen Gadolinium-basierten Vergleichspräparate vergleichbar, mit einer geringen Inzidenz interventionsbedingter Nebenwirkungen, und im Allgemeinen konsistent mit früheren Daten zu Gadoquatrane und anderen makrozyklischen Gadolinium-basierten Kontrastmitteln.